|
Pfannendachplastik mit kortiko-spongiösen Knochentransplantaten zur Therapie der Hüftgelenksdysplasie und Coxarthrose
Dieter Müller
In Kürze
Die Hüftgelenksdysplasie des Hundes kann vor dem Auftreten von arthrotischen Veränderungen beim wachsenden und jungen Hund sehr gut durch umstellende Beckenosteotomien (z.B. dreifache Beckenosteotomie) behandelt werden. Bei Patienten mit einer fortgeschrittenen Hüftgelenksarthrose und zerstörten Knorpeloberflächen kommen nach den allgemein anerkannten Behandlungs-Algorithmen nur eine Femurkopf- und Halsresektion oder eine Totalendoprothese in Betracht. In der bisherigen Behandlungssystematik klafft eine Lücke zwischen den Stadien, bei denen eine Beckenosteotomie nicht mehr in Frage kommt und den Endstadien, die nur mit einer Hüftgelenksprothese oder Amputation des Hüftgelenkkopfes zu behandeln sind. Die Pfannendachplastik mit einem autologem Knochenimplantat aus dem Os ilium schließt diese Lücke solange der Gelenkknorpel nicht zerstört ist. Der Eingriff sorgt für eine dorsale Abstützung des Femurkopfes und beseitigt erfolgreich Schmerzen, die durch eine Zerrung der Hüftgelenkskapsel ausgelöst werden. Der dorsale Acetabulumrand wird entlastet und durch Einwachsen des autologen Knochenimplantats direkt über der Gelenkkapsel verstärkt. Das am Transplantationsort einwachsende Knochengewebe formt einen neues dorsales Dach des Acetabulum; die Gelenkkapsel wird dadurch zu einem gewichtstragenden Bestandteil der Hüfte. Die Beschreibung der Technik beruht auf Erfahrungen, die der Autor in einem Zeitraum von 12 Jahren gesammelt hat, wobei 120 Patienten nachverfolgt werden konnten. 85 % der Patienten zeigten sehr gute Resultate und wiesen bis ins hohe Alter keine Schmerzrezidive auf. Sie benötigten keine zusätzliche antiphlogistische Behandlung oder chirurgische Therapie (Hüftgelenksersatz). Bei der orthopädischen Nachuntersuchung zeigten sich die operierten Hüftgelenke stabil. Die mit zunehmenden Lebensalter bisweilen sichtbaren Osteophytenbildungen blieben klinisch symptomlos. Die Resultate bestätigen, dass die Pfannendachplastik mit autologem Knochenspan bei entsprechender Indikationsstellung eine erfolgreiche Methode in der Behandlung des Hüftgelenksdysplasie-Coxarthrosekomplexes darstellt. Röntgenologisch konnte bewiesen werden, dass die Implantate nicht nur einwachsen, sondern der Kristallisationspunkt für weiteres Knochenwachstum sind. Unsere Langzeitresultate finden sich in Übereinstimmung mit den Ergebnissen, die Slocum (1998) in vergleichbarer Technik bei 300 Hunden veröffentlichte.
Behandlungsmethoden bei Hüftgelenksdysplasie und Coxarthrose
In der aktuellen wissenschaftlichen Literatur wird eine Vielzahl von chirurgischen Behandlungsmöglichkeiten der Hüftgelenksdysplasie und später daraus resultierender Coxarthrose genannt. Man unterscheidet dabei Verfahren, die den jungen Patienten vorbehalten bleiben von denen die beim ausgewachsenen Patienten angewendet werden. Hinzu kommen mehrere palliative Verfahren, die nicht kurativ sind sondern nur eine Symptomfreiheit oder Schmerzreduktion zum Ziel haben. Auf konservative Maßnahmen oder alternative Ansätze (Akupunktur) soll nicht eingegangen werden. Der Zeitpunkt der Diagnose „HD“ ist entscheidend für die Therapie.
Jugendlicher (immmaturer) Patient
Im Idealfall wird die dysplastische lockere Hüfte in einem möglichst frühen Stadium also im Alter von wenigen Monaten diagnostiziert. Hier besteht die Chance mit umstellenden Maßnahmen an den knöchernen Strukturen anatomische Fehlstellungen zu korrigieren sowie durch formative Reize im weiteren Wachstum die Gelenksituation nachhaltig zu verbessern. In den meisten Fällen liegt ein zu flaches Acetabulum mit wenig ausgebildetem dorsalen Acetabulumrand vor – hier wird vorzugsweise die
dreifache Beckenosteotomie
nach Slocum (DBO, engl. TPO) durchgeführt. Diesem Eingriff wird in der Literatur eine große Effektivität und Erfolgsrate bescheinigt. Bei tiefer Pfanne und steilem Hals (Coxa valga) ist eine
intertrochantäre Varisationsosteotomie
(ITO) nach Prieur zu bevorzugen. Gleichzeitig können Rotationsabweichungen des Femurhalses (Coxa valga antetorta) korrigiert werden. Auch dieser Eingriff ist kurativ bei einer geringen Komplikationsrate. In der Regel sind die weitere Entwicklung und Prognose günstig. Die
Femur-Halsverlängerung
nach sagittalem Einschnitt in den proximalen Femur durch Spreizung des Osteotomiespaltes mit Spezialkeilen, Knochenstücken oder einer Dehnschraube wird ebenfalls als korrigierende Maßnahme genannt (Slocum, 1998).
Adulter Patient
DBO und ITO sind solange keine arthrotischen Veränderungen vorhanden sind, bis zu einem Alter von ein bis zwei Jahren möglich. Bei Coxarthrosen sind sie kontraindiziert. Die nicht-amputativen Verfahren bei Coxarthrose wie
Pektineus-Myotomie
,
Pektineus- und Iliopsoasmyotomie
zusammen
mit ventraler Neurektomie „PIN“
(Ballinari, 1995) oder die so genannte
dorsale Denervation
(Neurektomie, Nervenschnitt; Kinzel, 1997) sollen eine möglichst weitgehende Schmerzausschaltung herbeiführen ohne an den insuffizienten knöchernen Strukturen der Hüfte etwas zu verändern. Dies hat zur Folge, dass die Verschleißprozesse am Hüftgelenk weiter fortschreiten. Ist der Gelenkknorpel weitgehend zerstört kommen nur noch die
Femurkopf- und Halsamputation
oder die
Endoprothese
in Betracht. Beide Verfahren sind etabliert und erfolgreich in der Beherrschung eines Endstadiums von Coxarthrose. Alternative Behandlungsansätze wie die
Goldimplantation,
welche als „Dauerakupunktur“ des Hüftgelenkes Wirkung zeigen soll, werden höchst kontrovers diskutiert. Unbestreitbar auch hier die Tatsache, dass bei der Goldimplantation keine Veränderungen an den knöchernen Strukturen des Hüftgelenks (etwa im Sinne einer Stabilisierung) erfolgen. In der bisherigen Behandlungssystematik fehlt ein operativer Eingriff, der die Lücke zwischen den gelenkerhaltenden knöchernen Umstellungsmaßnahmen (bei noch nicht ausgeprägter Arthrose) und den amtputativen bzw. gelenkersetzenden Verfahren füllt. Diese Behandlungslücke kann durch die Pfannendachplastik mit kortiko-spongiösen Knochentransplantaten geschlossen werden. Die überwiegende Zahl von Patienten mit Coxarthrose gehört dieser Zwischengruppe an und kann der Pfannendachplastik zugeführt werden. Von Vorteil sind die Erhaltung des natürlichen Gelenkes, die Verbesserung der Gelenkstabilität, die Schmerzausschaltung und die grundsätzlich offen gehaltene Option für einen eventuellen späteren Gelenkersatz.
Historie der Knochentransplantation am Hüftgelenk
Die Pfannendachplastik ist ein Verfahren, welches in der Humanmedizin seinen festen Platz hat. Als beispielhafte Indikation sei die Pfannendachplastik nach frühkindlicher Poliomyelitis genannt. Hierzu werden körpereigene Knochenspäne unterschiedlicher Größe und Mineralknochen auf natürlicher Basis (z.B. Pyrost®) eingesetzt.
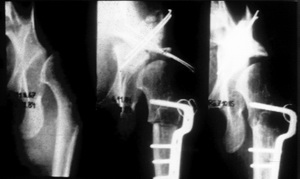
Pfannendachplastik in der Humanmedizin
Erstmals wurde die Appositionspfannedachplastik von Chiari in den zwanziger Jahren des letzten Jahrhunderts beschrieben.
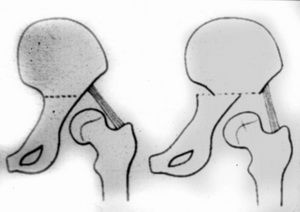
Chiari-Operation beim Kind zur Bildung eines künstlichen Pfannendaches
In der tiermedizinischen Literatur findet sich eine frühe Veröffentlichung von Dobbelaar (1962), der Auto- und Homotransplantate am Acetabulum zur Behandlung der Hüftgelenksluxation erfolgreich einsetzte.
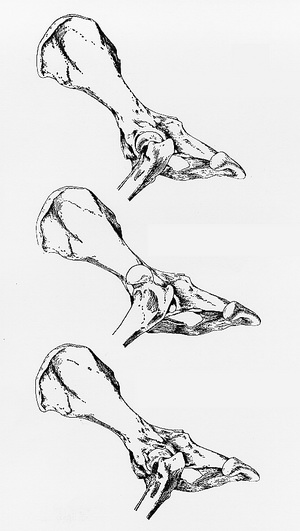
Knochentransplantate am Hüftgelenk nach Dobbelaar
Er untersuchte auch das weitere Schicksal der Transplantate an der Akzeptorstelle und stellte fest, dass diese verpflanzten körpereigenen Knochenbestandteile nicht abstarben sondern tatsächlich am oberen Acetabulumrand einwuchsen.
Funktion der Knochentransplantate nach Dobbelaar:
-
die körpereigenen Knochentransplantate stützen den Oberschenkelkopf ab
-
die Transplantate wachsen fest ein
-
es gibt keine Fremdkörperreaktionen oder Abstoßungsreaktionen
-
im weiteren Verlauf kommt es zu einer ausgeprägten Kallusbildung, die das Hüftgelenk weiter stabilisiert und dauerhaft schmerzfrei macht
Diagnose und Klassifikation bei Hüftgelenksdysplasie und Coxarthrose
Die Diagnostik umfasst die visuelle Beobachtung des Bewegungsablaufes, die klinische und radiologische Untersuchung sowie Funktionsteste. Beim Junghund stehen Hüftgelenkslaxheit, Tonusverlust und Krepitation des Gelenks im Vordergrund. Sie können mit dem Ortolani-Test klassifiziert werden. Die Laxheit des Hüftgelenks korreliert jedoch nicht mit den klinischen Symptomen und ist kein Vorhersagekriterium für spätere degenerative Gelenkserkrankungen und Coxarthrose. Beim adulten Hund sind die Ortolani-, Bardens- oder Barlowteste selten positiv. Aussagekräftiger ist die Schmerzreaktion des Patienten bei einer starken Extension des Gelenks, sie dient auch zur Abgrenzung einer lumbo-sakralen Stenose. Der juvenilen Lockerheit des Gelenks ist einer eingeschränkten Beweglichkeit gewichen mit periartikulärer Fibrose, Krepitation, Osteophytenbildung und einem zunehmenden Verlust der Tiefe des Acetabulum. Slocum und Slocum (1999) teilen die
Hüftgelenksveränderungen in sieben Klassen
ein:
1. Normales Hüftgelenk
Femurkopf immer kongruent im Acetabulum. Keine pathologischen Veränderungen. Dünne straffe Gelenkkapsel.
2. Subluxierendes Hüftgelenk
Femurkopf unter Normalbedingungen im Acetabulum. Jedoch Tendenz zur lateralen Deviation und gezerrter Gelenkkapsel.
3. Intermittierend subluxiertes Hüftgelenk
Bei Adduktion wird der Femurkopf aus dem Acetabulum gezogen. Lädierte überdehnte Gelenkkapsel.
4. Luxiertes aber reponierbares Hüftgelenk
Der Femurkopf befindet sich noch in der Gelenkkapsel luxiert jedoch bei Abduktion oder Rotation des Gelenks. Typisches Ortolani-Knacken. Dorsaler Pfannenrand, Gelenkkapsel sind beschädigt, Füllung des Acetabulums mit pathologischen Villi und Pannus. Periartikuläre Osteophyten.
5. Ausgeprägte aber reponierbare Luxation
Der Femurkopf liegt nicht mehr kongruent im Acetabulum. Bei axialem Druck kann er jedoch reponiert werden. Hüftgelenk ist instabil und luxiert spontan. Die Füllung des Acetabulums mit Osteophyten schreitet fort. Dorsaler Acetabulumrand wird extrem belastet und verschlissen. Hypertrophie des Lig. teres. Der mediale Anteil des hyalinen Knorpels des Kopfes trägt zunehmend die gesamte Belastung. Gefahr von Knorpeldefekten.
6. Nicht-reponierbare Luxation des Hüftgelenks
Der Femurkopf befindet sich innerhalb der Gelenkkapsel aber außerhalb des Acetabulum. Er kann nicht mehr in das Acetabulum zurückgedrückt werden. Osteophyten an Kopf und Hals. Abschleifung des dorsalen Acetabulumrandes. Beginnende Eburnation des Gelenkknorpels von Kopf und Pfanne. Allmähliche Ausbildung einer Knorpelglatze. Bei zerstörtem Knorpel ist eine Femurkopfresektion oder Totalendoprothese einzige chirurgische Option.
7. Vollständig luxierte Hüfte
Der Femurkopf ist vollständig luxiert. Er befindet sich außerhalb der Gelenkkapsel (Luxatio femoris). Möglich durch Trauma bei normalem Hüftgelenk mit relativ günstiger Prognose. Luxation auf Grund eines sehr flachen Acetabulums und fortgeschrittener Coxarthrose durch Überbelastung der Gelenkkapsel möglich. Ungünstige Voraussetzungen für Totalendoprothese. Femurkopf- und Halsresektion als ultima ratio.
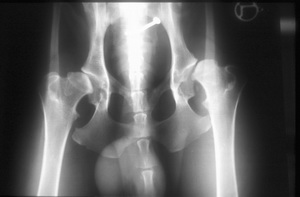
Subluxation beider Hüftgelenke; „lockere Hüfte“
Bedeutung des dorsalen Acetabulumrandes (DAR)
Beim dysplastischen Hüftgelenk tritt eine zunehmende Luxationsneigung des Femurkopfes auf. Er verlagert sich nach lateral und dorsal. Das Gewicht wird nicht mehr durch das knöcherne Acetabulum getragen sondern zunehmend durch die dorsalen Anteile der Gelenkkapsel. Der dorsale Acetabulumrand besitzt anfangs noch ausreichende Integrität, wird jedoch durch den Femurkopf beansprucht und traumatisiert. Die Kraftvektoren orientieren sich immer mehr Richtung dorsalen Rand und dorsaler Gelenkkapsel. Diese wird zunehmend ausgeweitet. Kompensatorisch tritt eine Kapselfibrose ein, die jedoch nach Abschleifen des dorsalen Acetabulumrandes das Gelenk nicht stabilisieren kann und ein Herausgleiten des Oberschenkelkopfes begünstigt. Die Synovilais der Articualtio coxae ist hochgradig entzündet. Wie in anderen Gelenken treten pathologische Villi auf.
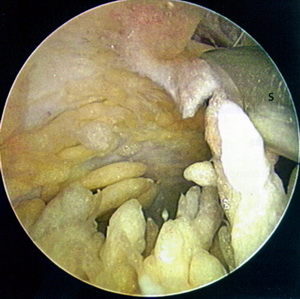
Pathologische Villibildung infolge Arthrose (Acetabular Filling)
Im Stadium 5 wird der Femurkopf nicht mehr durch das Acetabulum unterstützt, sondern nur noch durch die Gelenkkapsel und die umgebende Muskulatur. Die Adduktoren, besonders der M. pectineus, werden exzessiv gedehnt. Die Abduktion des luxierten Femurkopfes führt zu zusätzlichen Zugkräften auf die gedehnte und entzündete Gelenkkapsel – als Folge tritt ein starker Hüftgelenksschmerz auf.
Symptome
Die zunehmende Abrundung des Acetabulums begünstigt ein Herausgleiten des Femurkopfes in die luxierte Position. Bei geringer Belastung können die Abduktoren des Hüftgelenkes zusammen mit den Rotatoren den Oberschenkelkopf in der Reduktionsstellung halten. Die unphysiologische Belastung führt zu einer Ermüdung der Muskelgruppen und nachfolgenden Luxation des Hüftgelenkes. Durch eine bodenweite Stellung der Hintergliedmaße versucht der Hund sein Hüftgelenk im knöchernen Acetabulum zu halten. Die axialen Belastungskräfte drücken den Femurkopf in die Pfanne. Zu beobachten ist auch ein Wechsel zwischen bodenweiter und bodenenger Stellung. Beim Treppensteigen nimmt der Hund eine bodenweite Stellung ein. Beim Sprung in das Auto sind ein deutliches Zögern und sodann der Übergang zu einer bodenengen Stellung vor dem Absprung zu beobachten. Im Extremfall ist bei Hunden mit Hüftgelenksdysplasie ein gleichseitiges hasenartiges Hoppeln mit beiden Hinterbeinen zu sehen als Ausdruck einer hochgradigen Luxation und Degeneration der Hüfte.
Knochentransplantate
Knochentransplantate spielen eine bedeutende Rolle in der orthopädischen und wiederherstellenden Chirurgie. Man unterscheidet die Knochentransplantate nach Herkunft und Struktur: Ein
Autotransplantat
stammt von einer Stelle des Skeletts und wird an eine andere Stelle des gleichen Körpers übertragen. Ein
Allotransplantat
besteht aus Gewebe, welches von einem Individuum auf ein anderes Individuum der selben Spezies übertragen wird, welches genetisch gesehen nicht identisch ist. Ein
Alloimplantat
besteht aus nicht-vitalem Knochen, der zum Zwecke der Verpflanzung durch physikalische und chemische Verfahren so verändert wurde, das er bei einem anderen Individuum eingesetzt werden kann. Ein
Xenotransplantation
beschreibt die Transplantation von Gewebe auf ein Individuum einer anderen Spezies. Nach der Zusammensetzung unterscheidet man spongiöse, kortiko-spongiöse, knochenmarkhaltige, knöcherne (kortikale) und osteochondrale Transplantate.
Spongiosatransplantate
bestehen aus trabekulär angeordneten zellreichen Knochengewebe, welche aus der Markhöhle der langen Röhrenknochen im metaphysären Bereich entnommen werden. Ihr Hauptvorteil liegt in der Stimulation und Produktion von neuem Knochengewebe.
Kortikalistransplantate
bestehen aus dem dichten äußeren kortikalen Knochen und besitzen den Vorzug der strukturellen Stabilität.
Kortiko-Spongiosatransplantate
stellen eine Kombination beider Transplantate dar und enthalten neben der Kortikalis auch spongiöse Bestandteile, was sich positiv auf deren Integration auswirken kann.
Knochenmarktransplantate
enthalten lebende undifferenzierte mesenchymale Zellen. Ein Frischtransplantat wird unmittelbar nach der Entnahme wieder eingesetzt. Es kann sich dabei um freie oder vaskularisierte Transplantate handeln, die zusammen mit ihren Gefäßen an der Donorstelle entnommen und nach Anasthomosee mit den Gefäßen der Empfängerstelle als lebender Gewebeverband sofort funktional tätig werden können.
Funktion der Knochentransplantate
Knöcherne Transplantate werden benutzt um Defekte knöcherner Strukturen aufzufüllen, Substanzverluste an langen Röhrenknochen zu überbrücken, Gelenkfusionen nach Arthrodesen zu erreichen oder eine Frakturheilung bei so genannten „non unions“ herbeizuführen. Sie können jedoch auch als frei verpflanzte Ersatzknochen verwendet werden z.B. im Rahmen der wiederherstellenden kranio-fazialen Chirurgie oder im Bereich der Hüftgelenkspfanne bei zu gering ausgebildeter Gelenkskavität. Abhängig vom Typ des Transplantats bietet dieses vitale Osteoblasten, osteoinduktive Faktoren, mechanische Stabilität oder Leitschienenfunktion für neues Knochenwachstum.
Spongiöse Grafts
werden in der Regel gewonnen um lebende Zellen und Wachstumsfaktoren zu erhalten, die die Produktion von neuem Knochen durch den Körper anregen. Sie bieten wenig strukturelle Unterstützung.
Kortikale Grafts
werden in Fällen, in denen eine strukturelle Verstärkung notwendig ist, eingesetzt. Sie können homologen oder autologen Ursprungs sein, wobei letzterer zu bevorzugen ist.
Osteogenese
Die Bildung von neuem Knochen wird durch Donorzellen wie den Osteoblasten und Osteoklasten ausgelöst, die den Transfer an die Verpflanzungsstelle überlebt haben oder durch Zellen des Transplantatempfängers veranlasst (Olds, 1973). Die Osteogenese, die auf der Übertragung von lebenden Zellen beruht ist nur bei frischen Transplantaten möglich. Im Falle eines autologen Knochentransplantats lösen sie auch keine Immunantwort aus. Knochenspongiosa besitzt eine größere osteogene Potenz als kortikaler Knochen. Sie weist eine größere Oberfläche auf, die mit ruhenden Zellen, undifferenzierten mesenchymalen Zellen und aktiven Osteoblasten besetzt ist (Stevenson, 1999). Die undifferenzierten mesenchymalen Zellen finden sich im Knochenmark und in dem Trabekelwerk der Knochenspongiosa und können sich zu Osteoblasten entwickeln. Sie ergänzen die Funktion der lebenden osteogenen Zellen in der Transplantatmasse. Diese Transplantate werden sehr schnell revaskularisiert und ermöglichen das Überleben der transplantierten Zellen. Der Prozentsatz der überlebenden Zellen in einem frischen Knochentransplantat ist nicht genau zu ermitteln. In vitro Studien ergaben jedoch, dass mehr als 60% der Zellen bei Raumtemperatur in Kochsalzlösung bis zu 3 Stunden nach Entnahme überlebten. Die vitalen Zellen in frischen Knochentransplantaten beginnen fast sofort mit der Knochenproduktion. Die maximale Rate der Osteogenese findet man 8 Wochen nach der Übertragung.
Osteoinduktion
Unter der Osteoinduktion am Transplantationsort versteht man den Prozess, bei dem undifferenzierte mesenchymale Zellen sich in Osteoblasten umwandeln nachdem sie in Kontakt mit Knochenmatrix des übertragenen Knochengewebes gekommen sind. Sie können durch verschiedene Stimuli in Chondroblasten und Osteoblasten entwickeln, die proliferieren und eine knöcherne Matrix produzieren. Als Modulatoren fungieren viele Substanzen wie morphogenetisch wirkende Proteine, transformierende Wachstumsfaktoren, insulin-ähnliche Wachstumsfaktoren, Zytokine, Tumornekrosefaktoren und Prostaglandin E. Die mesenchymalen Zellen, die von der Empfängerstelle her gebildet werden entstammen vom Knochenmark, Endost, Periost und Bindegewebe (Stevenson, 1999).
Osteokonduktion
Unter der Osteokonduktion versteht man das dreidimensionale Einwachsen von Kapillaren, perivaskulärem Gewebe und mesenchymalen Zellen mit dem daraus resultierenden Einwachsen von neuem Knochen aus dem Empfängerbett in poröse Hohlräume (Spongiosa) oder um ein Knochentransplantat (Stevenson, 1999). Das Transplantat dient dabei als ein Gerüst für dieses Wachstum (Burchardt, 1987).
Strukturelle Festigkeit
Knochentransplantate, die eine strukturelle Festigkeit aufweisen sollen und gleichzeitig als eine mechanische gewichtsbelastete Abstützung dienen sollen bestehen in der Regel aus kortikalen Knochenteilen. Um die Stabilität des Transplantats in seinem Bett zu gewährleisten muß es an der Kontaktzone zum Empfänger fest verankert werden. Dies kann z. B. durch eine interne Fixation nach den Prinzipien der unterschiedlichen Osteosyntheseverfahren geschehen.
Knochentransplantate am Acetabulum
Das ideale Knochentransplantat ...
-
liefert osteogene Zellen, die neuen Knochen produzieren
-
liefert osteoinduktive Faktoren, die die Differenzierung zu Knochenzellen induzieren
-
dient als osteoinduktive Leitschiene beim Einwachsen von neuem Knochengewebe
-
bietet statische Unterstützung anatomischer Strukturen.
Die anatomischen Verhältnisse am dorsalen Pfannenrand des Acetabulums erfordern ein Transplantat das den Idealforderungen möglichst nahe kommt. Neben der sofortigen mechanischen Stabilität ist eine schnelle und möglichst umfangreiche Osteogenese, Osteoinduktion und Osteokonduktion notwendig.
Kortiko-Spongiosatransplantate
Von den allgemein akzeptierten Grundsätzen der Knochentransplantation bieten kortiko-spongiöse Transplantate den besten Kompromiss zwischen schneller Integration an der Akzeptorstelle und mechanischer Stabilität. Spongiöser Knochen wird wegen der leichten Zugänglichkeit und der ausbleibenden Schwächung tragender Röhrenknochen bevorzugt aus der Ala ossis ilii entnommen. Das Os ilium besteht aus dem kranial ziehenden großflächigen Darmbeinflügel (Ala ossis ilii) und dem kaudal zur Beckenpfanne ziehenden Corpus ossis ilii. Vom Tuber sacrale ausgehend entlang der Crista iliaca kann problemlos ein großflächiges Knochenstück aus dem Darmbeinflügel entnommen werden. Dieses Explantat weist kortikale und spongiöse Eigenschaften auf. Zusätzlich kann Spongiosa mit einem scharfen Löffel aus dem Corpus ossis ilii entnommen werden. Die Transplantate werden nach Anlegen eines tiefen kortikalen Schlitzes direkt oberhalb des Kapselansatzes an der dorsalen Acetabulumrinne zusammen mit Spongiosa implantiert. Die geforderte mechanische Festigkeit wird durch das in den Slot fest eingekeilte Knochenstück und eine dorsal abstützende Kortikalisschraube erreicht. Die Langzeitergebnisse beweisen, dass das kortiko-spongiöse Iliumtransplantat am Implantationsort nicht nur überlebt sondern durch Osteogenese, Osteoinduktion und Osteokonduktion zur Ausbildung eines neuen erweiterten knöchernen Pfannendaches führt und das Hüftgelenk dauerhaft stabilisiert.
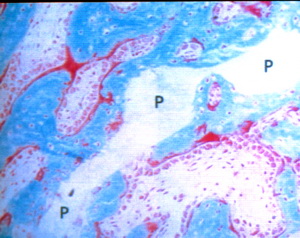
Intensive Knochenbildung (blaugrün) mit Osteoblastensäumchen (rot) um den verpflanzten Knochen
Die neue Knochensubstanz am Acetabulumrand wird als Antwort auf den mechanischen Stress während der Bewegung des Hüftgelenkes allmählich in kortikalen Knochen umgewandelt; ein Prozess, der mehrere Monate in Anspruch nimmt (Albrektsson, 1980).
Indikationen zur Pfannendachplastik
Die palliativen, symptomatisch ausgerichteten Verfahren (Neurektomie, PIN, Akupunktur, Goldimplantation, Pektineus-Myotomie) sollen in erster Linie (mit wechselhaftem Erfolg) schmerzausschaltenden Charakter haben. An der Biomechanik und den unphysiologischen Belastungsverhältnissen am dorsalen Acetabulumrand ändern sie nichts. Die Coxarthrose und der Gelenkverschleiß schreiten weiter fort - was den Einsatz dieser Verfahren insbesondere beim Junghund sehr problematisch erscheinen lässt. Wie ausgeführt fehlt in der bisherigen Behandlungssystematik ein operativer Eingriff, der die Lücke zwischen gelenkerhaltenden Umstellungs-Operationen und dem amputativen Verfahren bzw. der Hüftgelenks-Endoprothese schließt. Diese Lücke kann durch die Pfannendachplastik mit kortiko-spongiösen Knochentransplantaten geschlossen werden (Müller 1998, Slocum, 1998). Die Pfannendachplastik besitzt den Vorzug das natürliche Hüftgelenk zu stabilisieren und in den meisten Fällen lebenslange Schmerzfreiheit zu gewährleisten. Außerdem ist nach einer durchgeführten Pfannendachplastik jederzeit ein Hüftgelenksersatz möglich. In der Humanmedizin wird eine Pfannendachplastik bei flachem Acetabulum und damit unzureichender Verankerung der Polyäthylenpfanne als abstützende Maßnahme des eingesetzt.
Kontraindikationen der Pfannendachplastik
Beim nicht-maturen Patienten und bei Hunden bis zu einem (maximalen) Alter von zwei Jahren ohne arthrotische Veränderungen sind eher Umstellungsosteotomien indiziert. Aus Kostengründen kann jedoch auch hier eine Pfannendachplastik vertreten werden. Bei Zerstörung des Knorpelüberzuges des Oberschenkelkopfes und des Acetabulums (Knorpelglatzen) ist die Pfannendachplastik kontraindiziert.

Knorpelglatze des Caput femoris
Als operative Optionen kommen in diesen Fällen nur die Femurkopf und Hals-Resektion oder die Hüftgelenks-Endoprothese in Betracht.
Operationstechnik
Der Eingriff gliedert sich in zwei Schritte: Der Entnahme des kortiko-spongiösem Knochenspans aus dem Os ilium und dem Einsetzen des Implantates über der dorsalen Hüftgelenkskapsel.
Pfannendachplastik – Operationsschritte
-
Entnahme eines Knochentransplantat aus der Darmbeinschaufel
-
Anlegen einer halbkreisförmigen genau passenden Nut am oberen Pfannenrand
-
das Hüftgelenk und seine Kapsel werden dabei weder eröffnet noch verletzt
-
Implantation des zugerichteten Knochenspans und von Spongiosa
-
Primärstabilisierung der eingesetzten Implantate mit einer Schraube
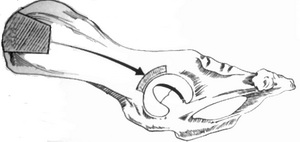
Verpflanzung des Knochentransplantates
Entnahme des Knochenspans
Der Zugang zum Darmbeinflügel erfolgt von kranio-dorsal (Matis u., Waibl H., 1999). Der Patient wird in Seitenlage fixiert. Der Eingriff erfolgt unter streng aseptischen Kautelen.
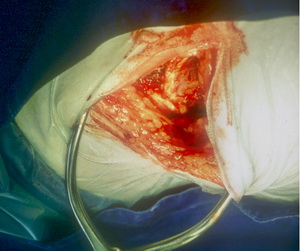
Entnahme des Knochentransplantates am Hüftbein
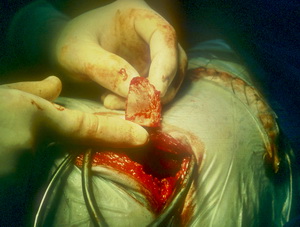
Entnommener Knochenspan
Die anfallenden Spongiosa- und Knochenspäne werden verwahrt. Der entnommene Knochenspan wird nun entsprechend der Abmessungen der angelegten Nut oberhalb der Hüftgelenkskapsel eingepasst. Die natürliche Wölbung des Transplantates passt sich gut der Kontur der dorsalen Gelenkkapsel an. Das Knochentransplantat muss einen perfekten und festen Sitz fest in seinem Bett haben. Eine Kortikalisschraube wird direkt über dem Transplantat angebracht und stabilisiert es während der Einheilungsphase.
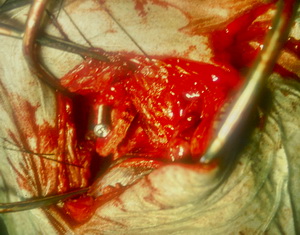
Implantierter Knochenspan mit abstützender Schraube
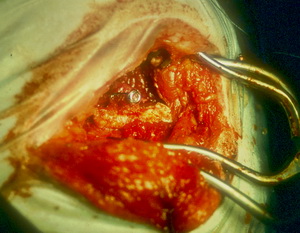
Die restliche Spongiosa und Knochenspäne werden zwischen Knochentransplantat und Gelenkkapsel implantiert. Sie haben eine wichtige Funktion bei der Integration des Transplantates und der Osteoinduktion.
Heilungsverlauf
Die Wundheilung erfolgt komplikationslos. Nach wenigen Wochen besitzt der Knochenspan eine feste Verbindung mit dem umgebenden Periost. Die Einheilung und Integration des Knochentransplantates erfolgen nach den beschriebenen Prinzipien. In den ersten sechs Wochen ist der Patient ruhig zu halten und nur an der Leine zu führen. Später kann die Belastung graduell gesteigert werden. Nach ca. 10 Wochen kann sich der Patient ungehindert frei bewegen. Die abstützende Schraube wird normalerweise nicht entfernt.
Indikation
Eine typische Indikation für die Pfannendachplastik stellt die Coxarthrose mit dem Bild des „Acetabular Filling“ dar. Slocum versteht darunter die allmähliche Füllung des Acetabulums mit Debris, welche dazu führt, dass der Oberschenkelkopf allmählich aus der Pfanne herausgedrückt wird.
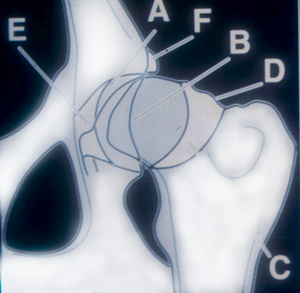
Sogenanntes „Acetabular Filling“ nach Slocum (A: inkongruentes Acetabulum; B: deformierter Pfannenrand, C: Osteophytenbildung; D: deformierter Hals und Kopf, E: Füllung des Acetabulumbodens, F: Osteophyten an kranialer Pfannenkontur).
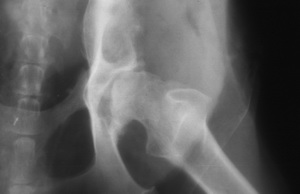
Äquivalent im Röntgenbild
Die nachfolgenden Abbildungen zeigen den typischen Verlauf bei einem Patienten, der an einer schmerzhaften Hüftgelenksarthrose litt. Er zeigte deutliche Lahmheitserscheinungen.
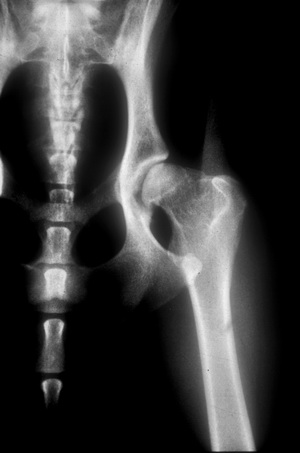
Hüftgelenksarthrose – Zustand vor der Operation
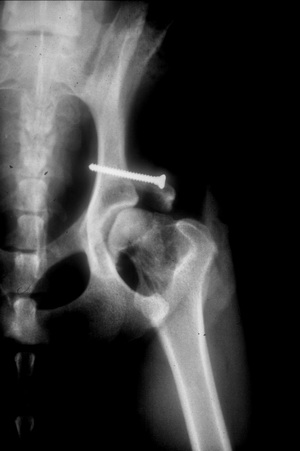
Pfannendachplastik unmittelbar nach der Operation
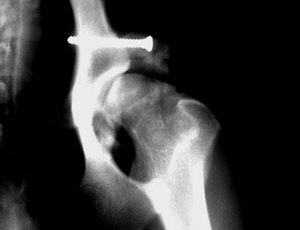
Zustand nach 1 Jahr. Das Transplantat ist integriert; die knöcherne Abstützung und Stabilisierung des Hüftgelenks ist erreicht.
Die Einheilung des verpflanzten Knochensegmentes ist röntgenologisch deutlich zu erkennen. Zugleich ist ein zusätzliches Knochenwachstum im Bereich des dorsalen Acetabulumrandes zu verzeichnen.
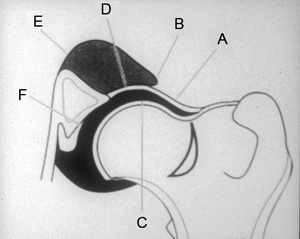
Gelenkkapsel, B: (schwarz) neues Acetabulumdach, C: Zentrum des Oberschenkelkopfes, D: Abgestütze Gelenkkapsel, E: Integrationszone des Implantates; F: „Acetabular Filling“ am Acetabulumboden.
Das Hüftgelenk wird nach der Operation zusätzlich durch die Gelenkkapsel („A“) und das neue Acetabulumdach („B“) getragen. Es hat sich ein neuer knöcherner dorsaler Gelenkrand gebildet und das Hüftgelenk luxiert nicht mehr. Ein weiterer Effekt der Pfannendachplastik ist in der dauerhaften Schmerzausschaltung zu sehen – dem Neurektomie-Effekt dieses Eingriffes. Die Patienten sind postoperativ trotz des eigentlich zu erwartenden Wundschmerzes weitgehend schmerzfrei. In vielen Fällen kann nach wenigen Tagen auf eine medikamenetöse Schmerztherapie verzichtet werden. Eine Erklärung für das schnelle Abklingen der Lahmheitserscheinungen nach der Pfannendachplastik ist neben der mechanischen Stabilisierung der Hüfte die dauerhafte Blockade der sensiblen von dorsal an die Gelenkkapsel herantretenden Nervenfasern durch die knöchernen Transplantate (Denervationseffekt im Sinne von Kinzel und Kürpper, 1997). Im Gegesatz zum reinen „Nervenschnitt“ sind Reinervationen und damit eine Wiederkehr der Schmerzleitung bei der Pfannendachplastik ausgeschlossen.
Komplikationen
Komplikationen in der postoperativen Phase sind sehr selten. An erster Stelle sind Wundheilungsstörungen und Infektionen der Wunde durch Belecken zu nennen. Das Tragen eines Halskragens über 14 Tage wird dringend empfohlen. Damit lassen sich diese Komplikationen vermeiden. Während des Einwachsens der Knochentransplantate kann es bei direkter und heftiger Gewalteinwirkung zu einer Lockerung des Knochentransplatates kommen, die unter Umständen zu einer Schädigung des N. ischiadicus mit nachfolgenden Nervenlähmungen führen können.
Gegenanzeigen
Die Pfannendachplastik ist nicht für Patienten geeignet, bei denen der Knorpelüberzug des Hüftgelenkes total zerstört ist also subchondraler Knochen auf Knochen reibt. Dies ist aber bei Hunden mit Hüftgelenksdysplasie und Coxarthrose nur in den meisten Fällen nicht der Fall. Bei der völligen Zerstörung der Gelenkknorpel kann nur der Einsatz einer Hüftprothese oder die Amputation des Oberschenkelkopfes (Femurkopfresektion) wirksame Schmerzbefreiung bringen.
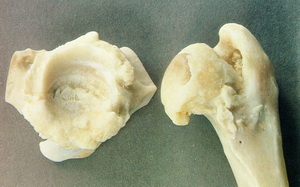
Ein völlig zerstörtes Hüftgelenk mit aufgeriebenem Knorpelüberzug ist nicht für eine Pfannendachplastik geeignet.
Ergebnisse
In einer retrospektiven Studie wurden die Operations- und insbesondere die Langzeitergebnisse betrachtet (Müller, 1998). Sie erstreckte sich über den Zeitraum von 1989 bis 1998. Die Daten wurden durch Befragung der Besitzer und wiederkehrende Untersuchungen der Patienten erhoben.
Die Einteilung erfolgte nach den Graden „gut“ (lahmheits- und beschwerdefrei, benötigt keine Antiphlogistika) – „befriedigend“ (gelegentliche Lahmheitsschübe, die unter NSAIDs wieder abklangen) – „unbefriedigend“ (benötigt im höheren Lebensalter zusätzliche NSAIDs) – und „schlecht“ (deutliche Lahmheit, Schmerzsymptomatik, die nicht hinreichend auf medikamentöse Behandlung anspricht) unterteilt. Letztere Patienten erhielten später entweder eine Hüftgelenksprothese, wurden einer Femurkopf- und Halsresektion unterzogen oder wurden aus Altersgründen euthanasiert.
Pfannendachplastik - Ergebnisse einer Langzeitstudie bei 120 Patienten
-
gut: 85 %
-
befriedigend: 10 %
-
unbefriedigend: 4 %
-
schlecht: 1 %
Die Ergebnisse decken sich mit den Resultaten von Slocum (1998) bei 300 Hunden. Dieser beobachtete 2 Monate postoperativ ein lahmheitsfreies Gangbild und Schmerzfreiheit. Die Gliedmaßenfunktion war völlig normal und es waren keine Subluxationen oder Luxationen des Femurkopfes mehr feststellbar. Zu beachten ist, dass die Abduktion der operierten Gliedmaße durch das vergrößerte knöcherne Acetabulumdach etwas eingeschränkt ist. Die Extensionsmöglichkeit des Hüftgelenkes nahm hingegen zu. Langzeitbeobachtungen: Bei der Autopsie von vier Hüftgelenken fand Slocum völlig stabile Gelenke vor. Die Gelenkkapsel hatte unter dem Knochenspan ihre rein kollagene Struktur verloren und war durch die Knochentransplantation fibro-kartilaginös verstärkt worden. Die Patienten hatten bis zum Zeitpunkt ihres Todes voll funktionale Hüftgelenke und benötigten auch im Alter keine Schmerzmittel. Slocum (1998) berichtete, dass aus seinem Patientengut über einen Beobachtungszeitraum von sechs Jahren kein einziger Hund Schmerzen entwickelte. Insbesondere erübrigte sich durch die herausragenden Erfolge der Pfannendachplastik der Einsatz von Hüftgelenksprothesen.
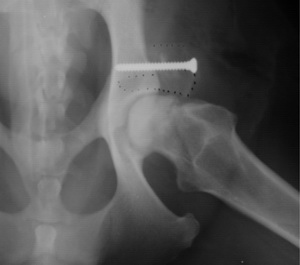
In 85 % der Fälle mit Hüftgelenksarthrose bringt die Pfannendachplastik gute bis sehr gute Erfolge und vermeidet den Einsatz einer Hüftgelenksprothese.
Fazit
Die Pfannendachplastik mit autologem kortiko-spongiösem Knochenspan füllt die therapeutische Lücke zwischen der dreifachen Beckenosteotomie und der Hüftprothese beim Hund. In der Beobachtung über einen Zeitraum von über zehn Jahren wurde bei 85% der Patienten ein gutes Ergebnis erzielt. Die Patienten hatten bis an ihr Lebensende ein funktionales Hüftgelenk, uneingeschränkte Lebensqualität und benötigten keine zusätzliche Schmerztherapie. Das autologe Knochentransplantat heilt nicht nur vollständig ein sondern wirkt zusätzlich osteoinduktiv. Die Patienten kommen lebenslang ohne die Gabe von schmerzstillenden Medikamenten oder den Einsatz von Hüftprothesen aus.
Anschrift des Autors
Dr. Dieter Müller
Fachtierarzt für Kleintiere, Chirurgie; Augenheilkunde
Kempener Str. 59
52525 Heinsberg
E-Mail: [email protected]
Literaturverzeichnis
-
Adams Wiliam M., Dueland R. T., et al: Early Detection of Canine Hip Dysplasia – Comparison of Two Palpation an Five Radiographic Methods, J Am Anim Hosp Assoc 34(4): 339-347 Jul/Aug 1998
-
Albrektsson T.: „Repair of Bone Grafts. A Vital Microscopic and Histopathological Investigation in the Rabbit”, Scand J Plast Reconstr Surg 14:1, 1980
-
Ballinari U., Montavon P. M. et al.: Die Pectineusmyektomie, Iliopsoastenotomie und Neurektomie der Gelenkkapsel als symptomatische Therapie bei der Coxarthrose des Hundes, Schweiz. Arch. Tierheilk. 137, 251-257, 1995
-
Burchardt H.: “Biology of Bone Transplantation”, Orthop Clin North Am 18:187, 1987
-
Cook James L., Tomlinson et al: Pathophysiology Diagnosis and Treatment of Canine Hip Dysplasia, Compend Contin Educ Pract Vet 18(8): 853-867 Aug 1996
-
Culvenor J. A., Parker R. J.: “Collection of Corticocancellous Bone Graft from the Ilium of the Dog using an Acetabular Reamer”, J Small Anim Pract 37(11): 513-515, Nov. 1996, Nov.
-
DaVid Thomas: “Apposition-Acetabuloplastics with Iliac Crest Autograft on Dogs. First Experience” Research Institute for Hip-Dysplasia, Vienna, Austria (1994).
-
Dobbelaar M. J.: “Osteoplastiek bj de Behandeling van de Luxatio Coxae van de hond”. Proefschrift Universität Utrecht, NL, 1962
-
Dobbelaar M. J.: “Dislocation of the Hip in Dogs”, J Small Anim Pract 1963; 4: 101.
-
Kinzel S., Küpper W.: „Operationstechnik und klinische Erfahrungen zur Hüftgelenksdenervation beim Hund“, Prakt. Tierarzt, Colleg. Veterinarium XXVII, S. 26 f., 1997
-
Matis U., Waibl H.: „Zugang zum Darmbeinflügel von kraniodorsal“ in: Schebitz, Brass – Operationen an Hund und Katze 2. Auflage S. 365, Parey Buchverlag 1999
-
Millis Darryl L., Martinez S. A.. „Bone Grafts“ in Slatter – Textbook of Small Animal Surgery 3rd edition, 1875-1891, 2003
-
Müller Dieter: “Fistelbildung nach Implantation des sogenannten biologischen osteoinduktiven Polymer (BOP)“ Herbstveranstaltung des Arbeitskreises für veterinärmedizinische Orthopädie, Tuttlingen Nov. 1991.
-
Müller Dieter: „Acetabulumplastik mit autologem Knochenspan beim Hund, Ergebnisse von 1989 bis 1998“ Vortrag. 44. Jahrestagung der Fachgruppe Kleintierkrankheiten der DVG, Stuttgart, Nov. 1998.
-
Olds R. B. et al: “Autogenous Cancellous Bone Grafting in Small Animals”, J Am Anim Hosp Assoc 9: 454, 1973
-
Sertl George O., Jensen D. J.: „SERTL Shelf Arthroplasty (BOP Procedure) in the Treatment of Canine Hip Dysplasia”, Vet Clinics of North America SA; Vol. 22 No. 3, May 1992.
Slocum Barclay, Slocum T. O.: “Femoral Neck Lengthening for Hip Dysplasia in the Dog”, Vet Surg 1989; 18:81
-
Slocum Barclay, Slocum T. O.: “Dorsal Acetabular Rim Radiographic View for Evaluation of the Canine Hip”, J Am Anim Hosp Assoc 26(3): 289-296 May/Jun 1990
-
Slocum Barclay, Slocum T. D.: “DARthroplasty” in M. Joseph Bojrab: Current Techniques in Small Animal Surgery 4
th
ed. 1998.
-
Staszky Carsten, Gasse H.: „Zur Innervation der Gelenkkapsel beim Hund, Teil 3 – Hüftgelenk“, Kleintierpraxis (47) Heft 1 S. 11-17, 2002.
-
Stevenson S.: “Biology of Bone Grafts”, Orthop Clin North Am 30: 543, 1999
|
